Magzatok fejlődnek a mesterséges anyaméhekben és létrehozták a rendszert is, ami vigyáz rájuk
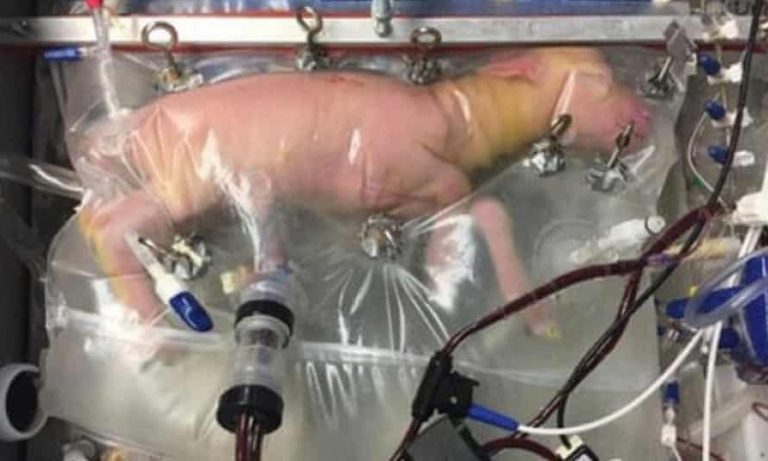
2017-ben a Nature Communicationben megjelent tanulmányban a Philadelphia Gyermekkórház munkatársai szokatlan, bár nem példanélküli kutatásról számoltak be: a laboratóriumban olyan, körülbelül száz napos bárány magzatokat vizsgáltak, amelyeket előzőleg kioperáltak az anyaméhből és áthelyeztek a biobag nevű mesterséges méhbe, hogy ott növekedjenek tovább. A bárányok átlátszó, meleg, tápanyagokat tartalmazó tasakban, az oxigént adagoló és a szén-dioxidot eltávolító készülék segítségével fejlődtek heteken át, miközben a kutatók felmérték, hogy az állatok vérkeringésére, tüdejére és egyéb paramétereire milyen hatással van az új környezet.
A kezdeti sikertelenségek után (a biobag korai verziójában az ötből három bárány szepszist kapott) a továbbfejleszett berendezéssel már közel egy hónapig is fenn tudták tartani a tesztalanyok egészségét és utána is csak azért kellett megszakítani a mesterséges "terhességet", mert a szabályok szerint ennél tovább nem lehetett életben tartani a magzatokat a kísérlet alatt. A nyolcból öt bárány 105-108 nappal a mesterséges méhbe való áthelyezése előtt fogant, és 25-28 napig tartózkodott a biobagben, míg három másik 115-120 napos volt és 20-28 napig élt a tasakban, mielőtt egy időre áthelyzeték őket egy lélegeztetőkészülékre, hogy a tüdejük állapotát ellenőrizzék. A mérések szerint ezek az állatok már nagyjából egészségesek voltak, normális tejsav és PH értékekkel, májfunkciókkal, nem lépett fel náluk vérszegénység és nem volt szükségük vérátömlesztésre sem. A megfelelő időben a szemüket is kinyitották, gyapjat növesztettek és szemmel látható módon növekedtek, egyre jobban kitöltve az átlátszó védőburkokat.
A biobag polietilén burkolata a fényt és a hangokat is áteresztette a jobb monitorozhatóság érdekében, a méretét pedig úgy tervezték meg, hogy minél inkább hasonlítson egy valódi méhre és egyúttal minimalizálják a magzatvíz mennyiségét is. Miután behelyezték a bárányokat és lezárták a burkot, a tasakokat átszállították egy mobil platformra, amely a folyadékok keringetését végezte és fenntartotta a megfelelő hőmérsékletet, valamint nyomást. A burok hangáteresztő képessége fontos, sőt döntő szerepet töltött be a magzatok egészségének megőrzése szempontjából, mivel lehetőséget adott az érintésmentes ellenőrzésre.
A magzatvizet imitáló folyadék a benne lévő tápanyagok és a sterilitás fenntartása, valamint a külvilágtól való védelem miatt nélkülözhetetlen hozzávalója a mesterséges méhnek, de egyúttal akadályt jelent a közvetlen beavatkozások során, ha arra kerül a sor. A tasak kinyitása vészhelyzetben ugyan lehetséges, de szennyező anyagok is bekerülhetnek ilyenkor, amelyek eltávolítása később problémát okoz. A biobagben növekvő állatot viszont ultrahanggal is lehet vizsgálni, így közvetlen érintkezés nélkül monitorozható az állapota.
A Philadelphiai Gyermekkórház kutatói a bárányokkal elért eredményeket a koraszülött emberi magzatok számára kifejlesztett mesterséges anyaméhek előállítására tervezték felhasználni, mivel az elsődleges céljuk a kezdetektől fogva a koraszülöttek életben maradási esélyeinek növelése volt azokban az esetekben, amelyekben a magzat nem túl fiatal a megmentésének megkísérléséhez, vagyis abban az életszakaszban van, ahol a kórházakban már jelenleg is megpróbálják megmenteni az életüket. Ennek érdekében azt is részletezték, hogy egy leendő, klinikai használatban lévő humán biobag hogyan nézne ki.
"Úgy gondoljuk, hogy a szülők számára megnyugvást jelenthet, hogy a magzatukat egy viszonylag védett, fiziológiai környezet tartja fenn.
A klinikai eszköz sok olyan funkcióval rendelkezik, ami lehetővé teszi a szülők számára, hogy kapcsolatban maradjanak a magzattal, köztük az ultrahanggal, a sötétben is működő kamerával, ami lehetővé teszi a magzat valós idejű vizualizációját az elsötétített környezetében, és a képességgel, hogy anyai szív-, és alhasi hangokat játszanak le a magzatnak. Ennélfogva úgy érezzük, hogy az előnyök messze túlszárnyalják a hátrányokat, amit a magzatnak a hagyományos ellátásnak való kitettsége jelent, amit az újszülött intenzív osztályok környezete a kritikusan koraszülött csecsemőkre ró." - írják a tanulmányban a kutatók.
A Guardian 2020-as beszámolója szerint a Philadelphiai Gyermekkórház találmányát néhány éven belül emberi felhasználásra is tervezték alkalmazni, és az FDA engedélyeztetésre is belátható időn belül sort akartak keríteni, de egyelőre még nem jelent meg a kórházakban az általuk készített mesterséges méh, és az IEEE Spectrum 2021-es megkeresésére sem reagáltak. A fejlesztések hosszas időt vehetnek igénybe, mivel olyan bonyolult kérdéseket is meg kell válaszolni, hogy vajon a placenta hiánya jár-e valamilyen egészségügyi hátránnyal vagy hogy hogyan lehet néhány hétnél jóval hosszabb ideig fenntartani a megfelelő környezetet a magzat számára.
Nem a biobag azonban az egyetlen mesterséges méh, amelyet a laboratóriumokban fejlesztenek, számos helyen zajlanak nagyon hasonló kutatások, ahol általában szintén bárányokkal vagy kecskékkel, időnként egerekkel tesztelik a rendszer működését. Az állatokat a néhány napos-hetes kísérleti időszak után nem hagyják tovább életben, az utólagos vizsgálatok során pedig adatokat gyűjtenek arról, hogy a szerveik fejlődésére milyen hatást gyakorolt a mesterségesen fenntartott környezet. Egy esetben azonban kivételt tettek a kutatók: George Mychaliska, a Michigan Egyetem gyermekgyógyászati sebésze, aki Robert Bartlettel, az első mesterséges méh feltalálójával együtt olyan, saját tervezésű berendezést készített, ami nem tartalmazott magzatvizet, egyszer szabadon engedett egy bárányt, amely előtte a mesterséges méh lakója volt. Az állat idősebb volt, mint a tesztek során általában használt alanyok (130 napos magzatként került a méhbe), és csak három napot töltött a berendezésben, ezért az ő esetéből nem vonhatóak le általános következtetések a hosszabb távú alkalmazás hatásaival kapcsolatban, de annyi biztos, hogy egészségesen került ki a mesterséges méhből és további öt évig élt, miközben két utódja is született.
A még megválaszolatlan orvosi kérdések mellett etikai kétségek is felmerülhetnek a biobagszerű eszközök jövőjével kapcsolatban, főként, ha nem csak a koraszülöttek életbentartására, hanem esetleg a terhességek általános helyettesítésére is tervezik használni majd, de egyelőre még távol állnak a fejlesztések attól, hogy ez utóbbinak az engedélyezése terítékre kerüljön. Azt azonban már lehet tudni, hogy hogyan válik megbízhatóbbá a rendszer, és hogyan lesznek nagyobb biztonságban a növekvő magzatok a berendezéseken belül, akár folytonos emberi felügyelet nélkül is.
A South China Morning Post beszámolója szerint kínai kutatók olyan mesterséges intelligencia programot terveztek, ami ellátja az ellenőrzés feladatát a hosszú távú növekedési folyamat alatt, ezzel extra védelmet nyújt a potenciálisan bekövetkező hibák ellen. A rendszer jelenleg egérembriókat felügyel, amelyek mesterséges magzatvízzel feltöltött tartályokban fejlődnek, az MI rendszer pedig éjjel-nappal monitorozza az állapotukat és szükséges szerint módosítja a berendezés beállításait. Baj esetén értesíti az emberi személyzetet, akiknek így kevesebb időt kell a közvetlen ellenőrzésekkel tölteni. Alacsony nagyítású és magasabb felbontású, nagyobb nagyítási képességű optikai modulokkal gyűjt adatokat az embriók elhelyezkedéséről és az algoritmusok segítségével online nyomkövetést tesz lehetővé.
A kutatók szerint ezzel akár egy, a hagyományos terhességnél biztonságosabb környezetet teremthet a magzatok számára, de egyelőre még nem tisztázott, hogy a hosszú távú növekedési folyamat végén vajon egészséges állatok láthatnának-e napvilágot.
(Fotó: Pxhere, Nature/Emily A. Partridge et al)



