A legnehezebben kezelhető rákos megbetegedések gyógyítására találtak új módszert az ELTE kutatói
Az ELTE PIT Bioinformatikai Csoportjanak kutatói, Grolmusz Vince professzor vezetésével a rákgyógyítás ígéretes formájának területén értek el nagy előrelépést, ami megnyithatja az utat a legnehezebben kezelhető rákfajták orvoslása előtt. A módszer alapját a mutálódott fehérjék kötéseinek helyreállítása és ezzel a korlátlan sejtosztódás megakadályozása adja, amihez a kötésre alkalmas kismolekulákat sikerült felfedezniük a kutatóknak.
Ahogy azt az International Journal of Molecular Sciences című lapban publikált tanulmányban írják: a különféle rákos daganatok kialakulásához legalább 600 fajta mutáns gén járulhat hozzá, legalábbis ennyit ismernek jelenleg a szakértők. Az esetek 25%-ában azonban fellelhető egy közös vonás: a RAS gének és ennek következtében a RAS fehérjék mutációja, ami a legsúlyosabb és legnehezebben gyógyítható ráktípusok kialakulása mögött húzódik meg. A RAS (rat sarcoma virus) fehérjének három izoformája létezik, a KRAS, a HRAS és az NRAS. Ezek közül a KRAS mutációja a leggyakoribb, főként hasnyálmirigyrák, vastagbélrák és tüdőadenokarcinómás esetekben, emiatt a gyógyszerfejlesztések során sokszor a KRAS-t célozzák.
A mutáns RAS fehérjék daganatkeltő hatása egy rendhagyó jelenségre vezethető vissza: a RAS és a GAP (GTPase-activating protein) fehérjék interakciójának zavarára. A RAS normál esetben a GAP-hoz kötődik olyan módon, ami a kellő feladatok elvégezése után leállítja a jelátvitel folyamatát. A mutálódott KRAS-nál a GAP-kötés nem megfelelő és a jelzés nem áll le, ami a sejtnövekedési faktorok kontrollálatlan gyártásához vezet. A korlátlan sejtosztódás következményeként pedig kialakul a rákos daganat.
A megoldást a RAS és a GAP mesterséges "összeragasztása" jelentheti, amihez megfelelő kismolekulákra van szükség. Az ELTE kutatói ezeket a molekulákat igyekeztek megtalálni, olyan módon, hogy a megfelelően közel elhelyezett RAS és GAP molekulák közé helyeztek jól kötő kismolekulákat. Az alábbi ábra azt a mesterségesen létrehozott RAS-GAP konfigurációt mutatja, amelyben a két molekula közötti résbe kerestek és találtak a kutatók jól kötő molekulákat, a piros v vektor mutatja a mesterségesen létrehozott eltolást.
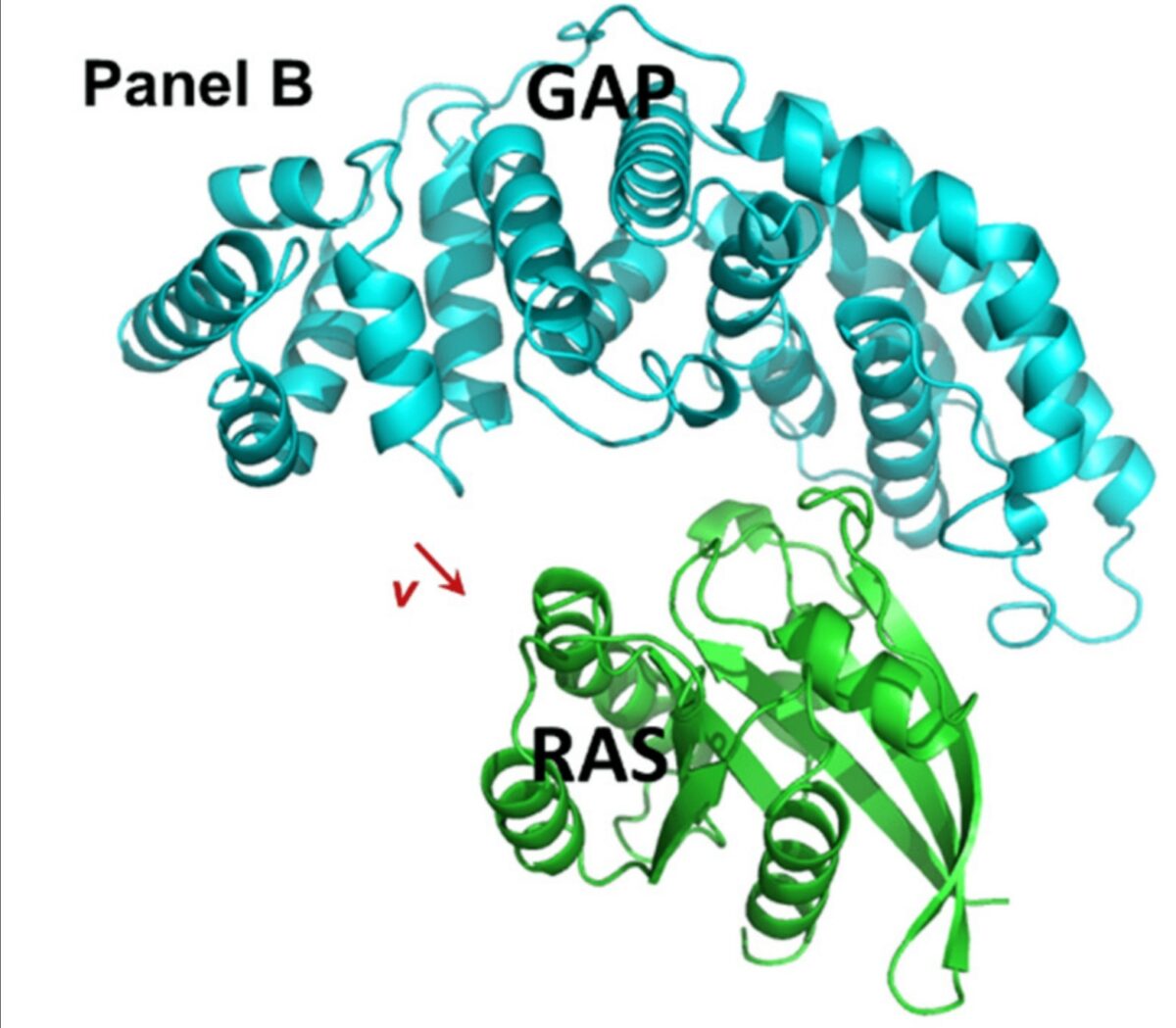
A kísérlet során a GAP és a mutáns KRASG12D molekulák közti ideális kötőelemet igyekeztek azonosítani a kutatók és sikerült két ígéretes kismolekulát, a 10-es és 14-es összetevőt, megtalálni, amelyek megakadályozták a humán hasnyálmirigyrák KRASG12D mutációjú PANC-1 sejtjeinek növekedését. A kismolekulák által kialakított kötések nem kovalensen kötnek, ami jobb megoldást jelent a gyógyszerek alkalmazásának szempontjából.
"A kutatók mintegy 30 éve próbálnak a mutáns RAS fehérjékhez gátló kismolekulákat kötni, azonban egészen a legutóbbi időkig kevés sikerrel.
Nemrég ugyan sikerült olyan molekulákat találni (ARS-853,ARS-1620), amelyek kovalensen, azaz nagyon erősen kötnek a RAS fehérjéhez, de a legtöbb gyógyszermolekula (így a ma használt antibiotikumok) nem kovalensen köt a célmolekulához, így az ARS molekulák nem optimális gyógyszerkandidátusok." - írják az egyetem beszámolójában.
A kutatók több magyar intézmény (KINETO Lab Kft, Országos Onkológiai Intézet, Semmelweis Egyetem, Budapesti Műszaki és Gazdaságtudományi Egyetem, HUN-REN Molekuláris Élettudományi Intézet, Uratim Kft.) segítségével igazolták, hogy az általuk alkalmazott megközelítés segítségével potens gyógyszerkandidátus molekulákat lehet találni.
"Az előzetes eredmények azt mutatják, hogy az új magyar módszer alapján talált legjobb két kis "ragasztó" molekula felveszi a versenyt a világon eddig talált legjobb hasonló molekulákkal."
- összegzi az ELTE - "A kutatók bíznak benne, hogy a munka folytatásával a leghalálosabb rákok ellen hatékony, kevés mellékhatással rendelkező új gyógyszereket találnak majd, hiszen a módszerrel nem a sejtosztódás alapvető mechanizmusaiba avatkoznak bele, mint a mai kemoterápiás beavatkozások, hanem a fiziológiailag normális állapotot állítják helyre."
(Fotó: Andrzej Wojcicki/Getty Images, ELTE, Grolmusz et al)
Itt állíthatod be, hogy a Rakéta az elsők között legyen a Google keresőben