Elkészült Barabási Albert Lászlóék koronavírus gyógyszerlistája a hálózati orvoslás eszközeinek segítségével
Végül elkészült a hálózati orvosláson alapuló, a Covid-19-hez felhasználható, már bevezetett és engedélyezett gyógyszerek listája, ami ezen a linken tekinthető meg. A kutatás megállapításainak megvitatására a résztvevők április 20-án, hétfőn, magyar idő szerint 17:00 órakor regisztrációhoz kötött eseményt rendeznek, amire itt regisztrálhatnak, az érdeklődők.
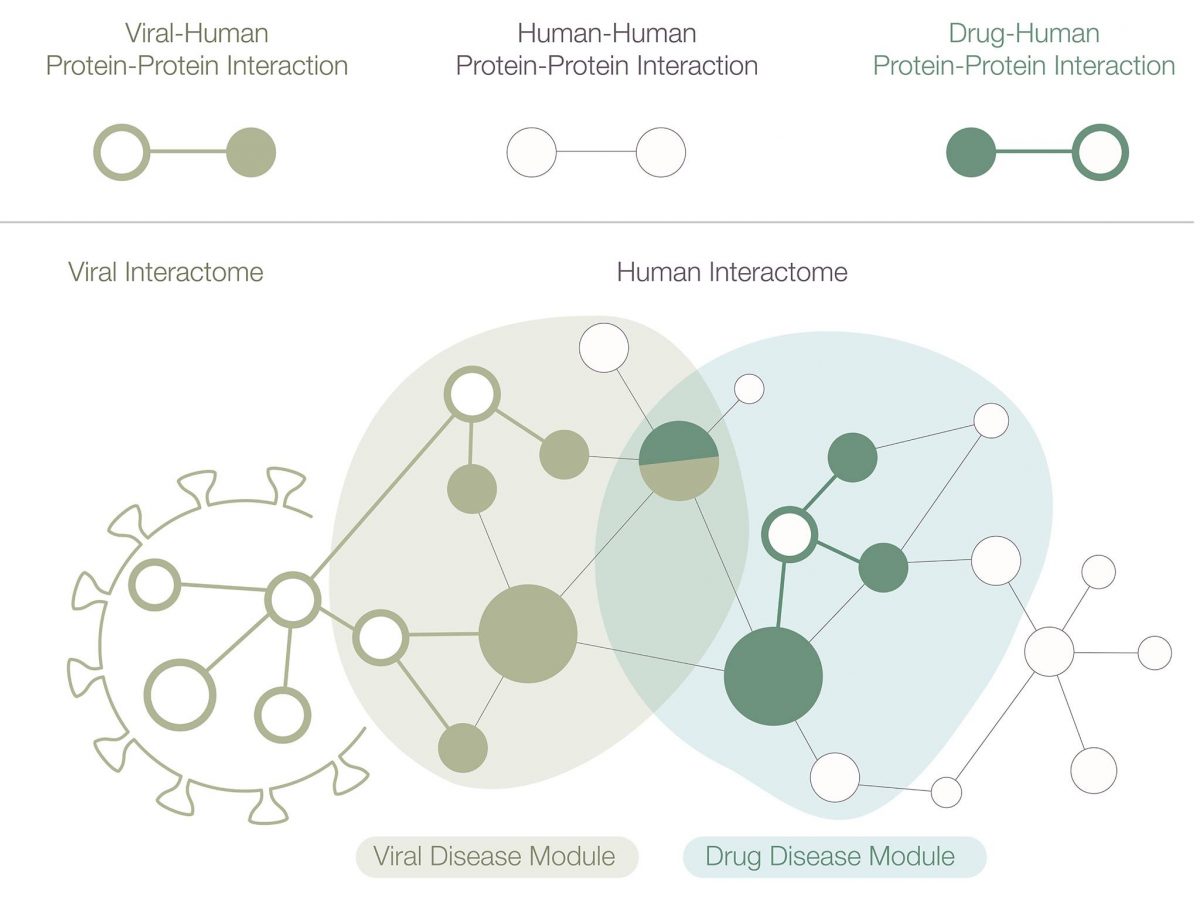
A hálózati orvoslás megközelítése a vírusfehérje-emberi fehérje és a gyógyszer hatóanyagok-emberi fehérje kölcsönhatásokat térképezi fel, az emberi interaktómában (fehérje-fehérje kölcsönhatások), hogy azonosítsák azokat a gyógyszereket, amelyek megzavarják a COVID-19 betegségmodul környezetét.
A hálózati orvoslás a hálózatok tudományának alkalmazása a betegségek azonosítására, megelőzésére és kezelésére. Ez a terület a hálózati topológia és a hálózati dinamika felhasználására összpontosít a betegségek azonosítása és az orvosi gyógyszerek fejlesztése céljából. A hálózati orvoslás felhasználja a biológiai hálózatokat, például a protein-protein kölcsönhatásokat és az anyagcsere útvonalakat. A betegséghálózatok, amelyek feltérképezik a betegségek és a biológiai tényezők közötti kapcsolatot, szintén fontos szerepet játszanak a területen. Az epidemiológiát széles körben vizsgálják a hálózati tudomány felhasználásával, a Hálózati Orvoslásban a közösségi- és közlekedési hálózatok a betegségek emberi populációkban történő terjedésének modellezésére szolgálnak. A hálózati orvoslás a rendszerbiológia orvosi szempontból koncentrált területe . A terület kezdőknek szánt bemutatása itt található: Network Medicine: a gentle introduction.
Mi a Network Medicine?
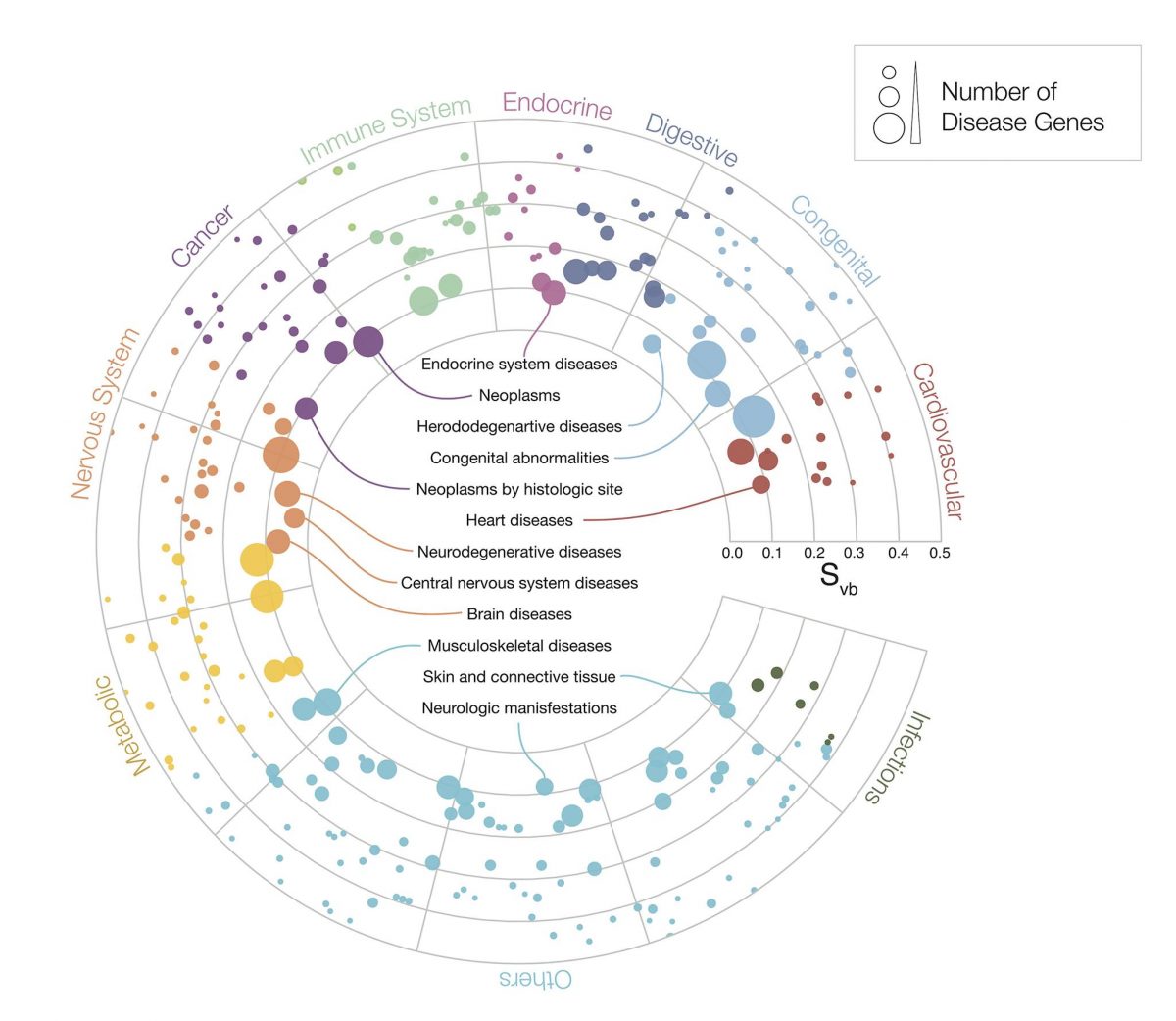
A betegség (COVID modulus) várhatóan a tüdő-, szív- és érrendszeri szövetekben, több agyi régióban, emésztőrendszerben (vastagbél, nyelőcső, hasnyálmirigy) és a reproduktív rendszer szöveteiben (hüvely, méh, herék, méhnyak, petefészek) fejti ki hatását (expresszálódik), és többszörös komorbiditást (társuló betegségek együttes előfordulása, kettő vagy több rendellenesség fellépése egy időben egy személynél) okozhat.
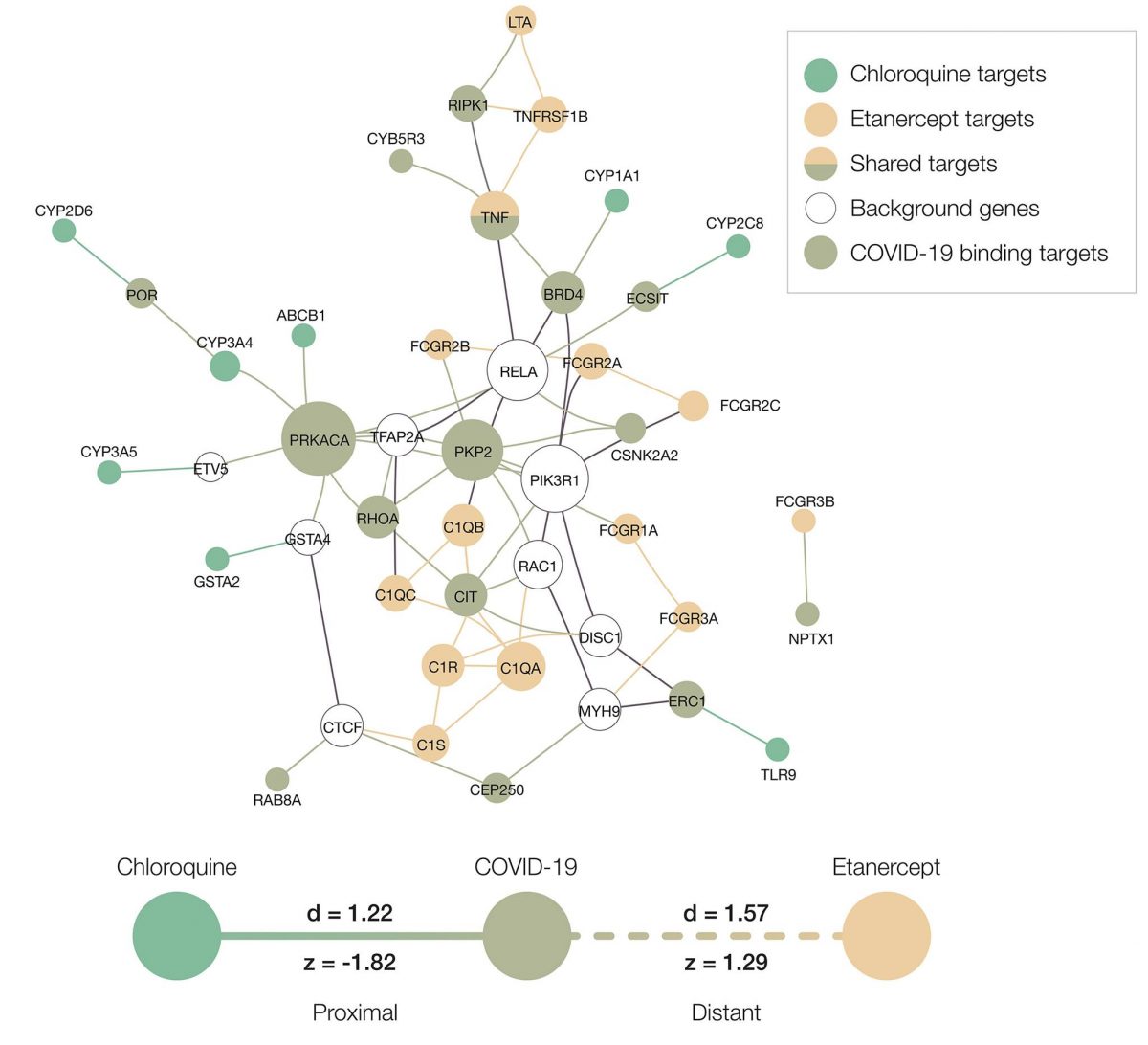
A kutatók három gyógyszer-újrahasználati stratégiát alkalmaztak, melyek során a hálózati közelséget, a diffúziót, és a mesterséges intelligenciát vették alapul, mindegyik megközelítésben rangsorolva a már jóváhagyott gyógyszereket, valószínű hatékonyságuk alapján a COVID-19 betegek esetében. Az említett módszertanok prediktív képességükben ugyan különböznek, de kombinálva őket, a három megközelítés szintézisét, a legjobb teljesítményt kapták.
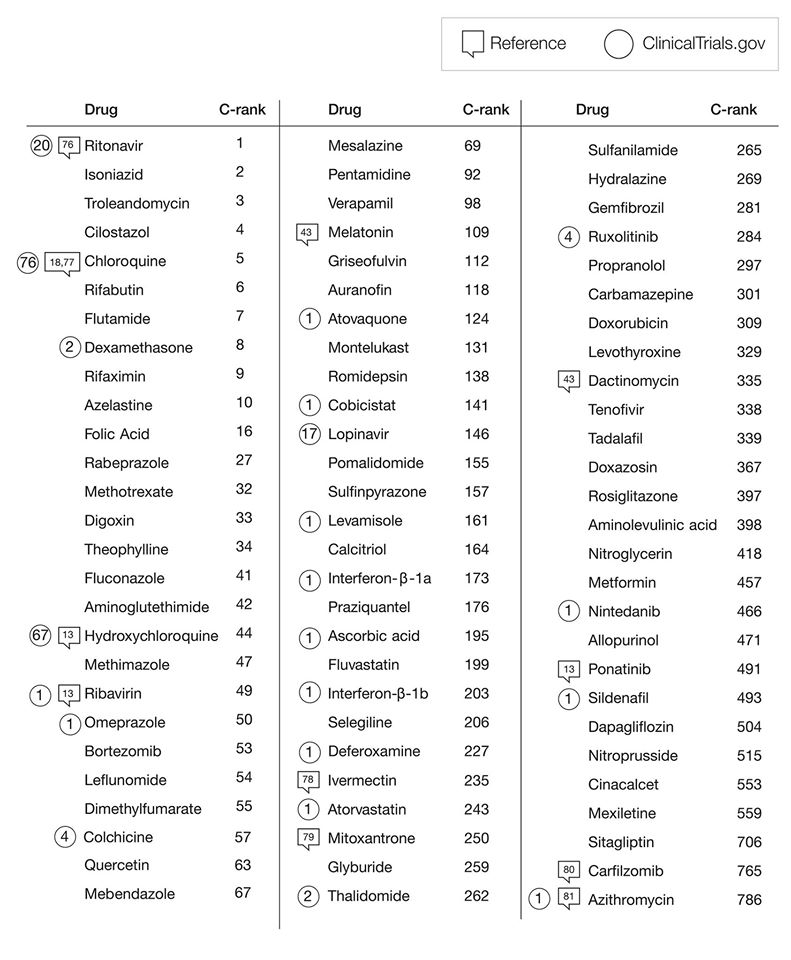
Joseph Loscalzo kutató manuálisan is megvizsgálta az összesített ranglistát, eltávolítva a felesleges és mérgező kábítószereket, és így született meg a 86 forgalomban lévő, bármikor felhasználható gyógyszert tartalmazó COVID-19 gyógyszerújrahasználati lista.
A Barabási Lab kutatói már megrendelték azokat a vegyületeket, melyek a gyógyszerek emberi emberi sejtekben történő teszteléséhez szükségesek, és remélik, hogy az ígéretesnek bizonyuló jelöltek hamarosan klinikai vizsgálatba kerülhetnek.
A betegségekkel kapcsolatba hozható fehérjék rendszere ún. betegségmodult alkot, ez lényegében egy gráf, amely tartalmazza a betegséggel kapcsolatba hozható valamennyi molekuláris szintű összetevőt. A betegségmodulok ilyen értelmű azonosítása lehet az első lépés a komplex betegségek molekuláris mechanizmusának megértéséhez.
Mi a betegségmodul?
A kutatók - nyilvánosan közzétéve a listát - felhívják a területen dolgozó szakembereket, hogy ne várjon senki rájuk - ha bárkinek rendelkezésre áll képzettség, eszköz, környezet a tesztelésére, gyorsan kezdjen bele! Emellett felajánlják segítségüket is, ha valahol teszt indul a lista alapján, várják a megkereséseket, készek részt venni a folyamatban! Ahogy Barabási professzor fogalmaz: Ez az utazás kezdete, nem pedig a vége!
“A hálózati gyógyászat lehetővé teszi számunkra, hogy jellemző profilt készítsünk bármely gyógyszer vagy gyógyszercsalád potenciális hatékonyságáról, függetlenül attól, hogy szerepel-e a végleges listánkban. Mindegyik gyógyszerhez gyorsan elkészíthető az egyoldalas profil, hogy kiderüljön annak molekuláris kapcsolata a COVID-19-hez (ha van ilyen kapcsolat).
A molekuláris biológiában az interaktóma a molekuláris interakciók összessége egy adott sejtben. A kifejezés kifejezetten a molekulák közötti fizikai kölcsönhatásokra utal (például a fehérjék között, más néven a protein-protein interakciók, PPI-k, vagy kis molekulák és fehérjék között), de leírhatja a gének közötti közvetett kölcsönhatások halmazát (genetikai kölcsönhatások) is. A szót eredetileg 1999-ben egy francia tudóscsoport hozta létre, Bernard Jacq vezetésével. Az interaktómák matematikai szempontból általában grafikonként jelennek meg, és noha az interaktómákat biológiai hálózatokként lehet leírni, ezeket nem szabad összekeverni más hálózatokkal, például az idegi hálózatokkal vagy a tápláléklánccal. Bármely betegség általában nem egyetlen gén hibájának következménye, jellemzően multiplex molekuláris folyamatok konzekvenciájaként értelmezhető. E folyamatok kapcsolatait az ún. interaktóma kódolja, egy hálózat, amely adott sejt valamennyi fizikális „interakcióját” integrálja, a fehérje-fehérje, a fehérje-DNS és a metabolikus interakciókat egyaránt.
Mi az Interaktóma?
A projekt csapatában, és a szélsebes eredmények előállításában az alábbi kutatók vettek részt: Deisy Morselli Gysi , Ítalo Do Valle , Marinka Zitnik , Asher Ameli , Xiao Gan , Onur Varol , Helia Sanchez , Rebecca Marlene Baron, Dina Ghiassian , Joseph Loscalzo , Albert-László Barabási és Alice Grishchenko grafikus designer, adatvizualizációs szakértő, valamint a KorganLab kutatói.
A Covid-19 gyógyszerújrahasznosításának más ígéretes, hálózati alapú megközelítéseiről, ezen és ezen a linken lehet tájékozódni.
(Forrás: BarabásiLab Képek: Barabási Lab, Unsplash)
Itt állíthatod be, hogy a Rakéta az elsők között legyen a Google keresőben