Felfedték a nehézsúlyú szuperbaktériumok antibiotikum-rezisztenciájának titkát
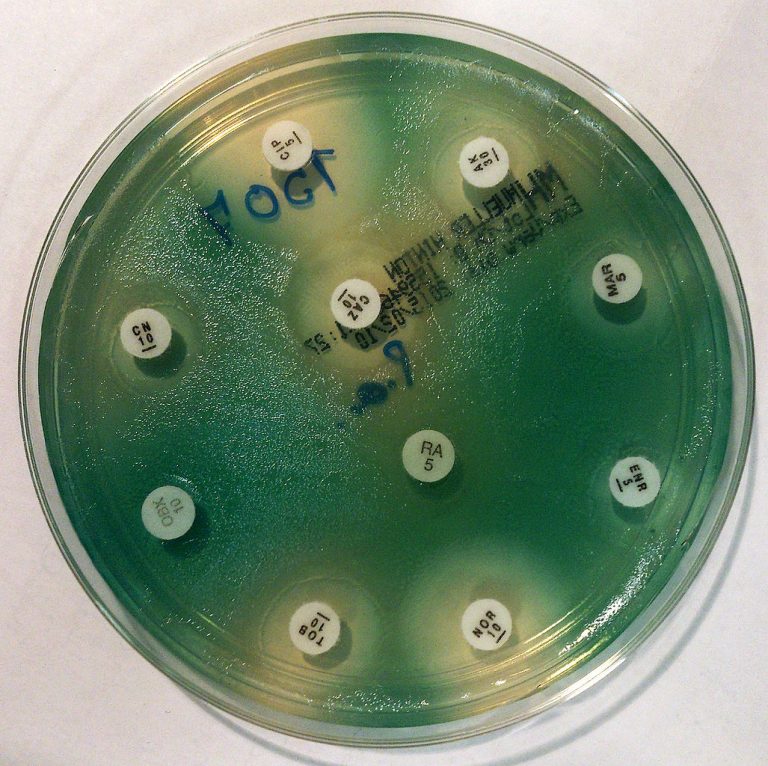
Kórházi fertőzések
A kórházi fertőzéseket olyan "szuperbaktériumok" okozzák, melyek az ellátóintézményekben petri-csészének használják, az ott koncentráltan megjelenő legyengült ellenállóképességű emberállományt. A kórokozók gyors evolúcióval szereznek ellenállóképességet a legfőbb védelmünket jelentő antibiotikumokkal szemben. A védekezéshez elengedhetetlen, hogy megtudjuk, hogyan csinálják.
A Pseudomonas aeruginosa egyike annak a három legfontosabb kórokozónak, amelyet az Egészségügyi Világszervezet "kritikusan fontosnak" tart az új antibiotikumok hatásosságának szempontjából. Ez a nehezen kezelhető, opportunista kórokozó, számos gyógyszerrel szemben képes gyorsan kifejleszteni az ellenállóképességet, ideértve a nagy teljesítményű „utolsó lehetőség” karbapenem antibiotikumokat is, és így nagy veszélyt jelent az emberi egészségre.
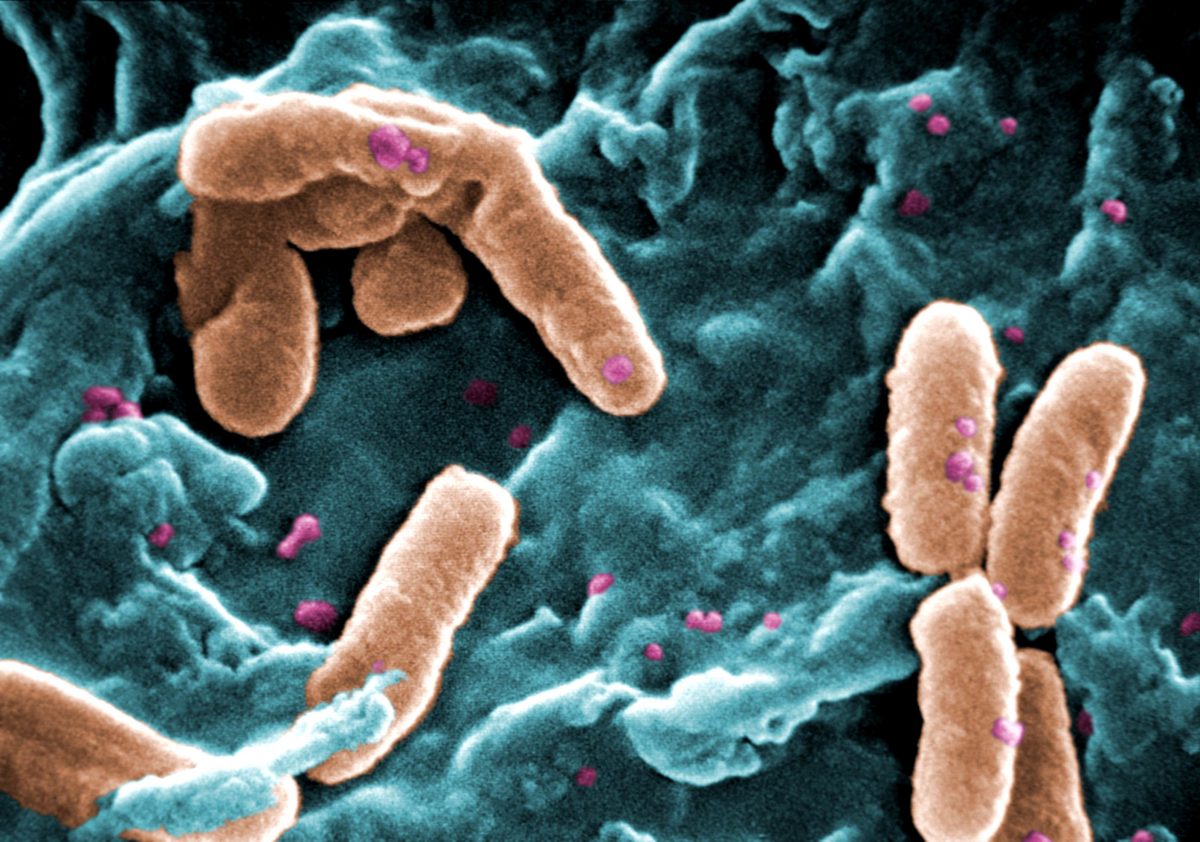
Az új gyógyszerek kifejlesztése mellett, a tudósok számára döntő jelentőségű az antibiotikum-rezisztencia kialakulását és terjedését okozó tényezők jobb megértése. A Nature Communications által közzétett új genomikai tanulmány azonosította a plazmidok egy olyan családját (a DNS kicsi kör alakú részeit, amelyek a kromoszómáktól függetlenül replikálódnak és átvihetők más baktériumokba), amelyek felelősek a P.aeruginosa multi-hatóanyag ellenállásának globális terjedésében, mely legalább az 1970-es évek óta tart.
A harmadik generációs genom szekvenálási módszerrel, amelyet long-read sequencingnek hívnak, a kutatók képesek voltak jellemezni egy kialakuló megaplazmid (nagy méretű plazmidok) családot, amely hozzájárult a P. aeruginosa multi-gyógyszeres rezisztenciájának elterjedéséhez egy thaiföldi kórházban.
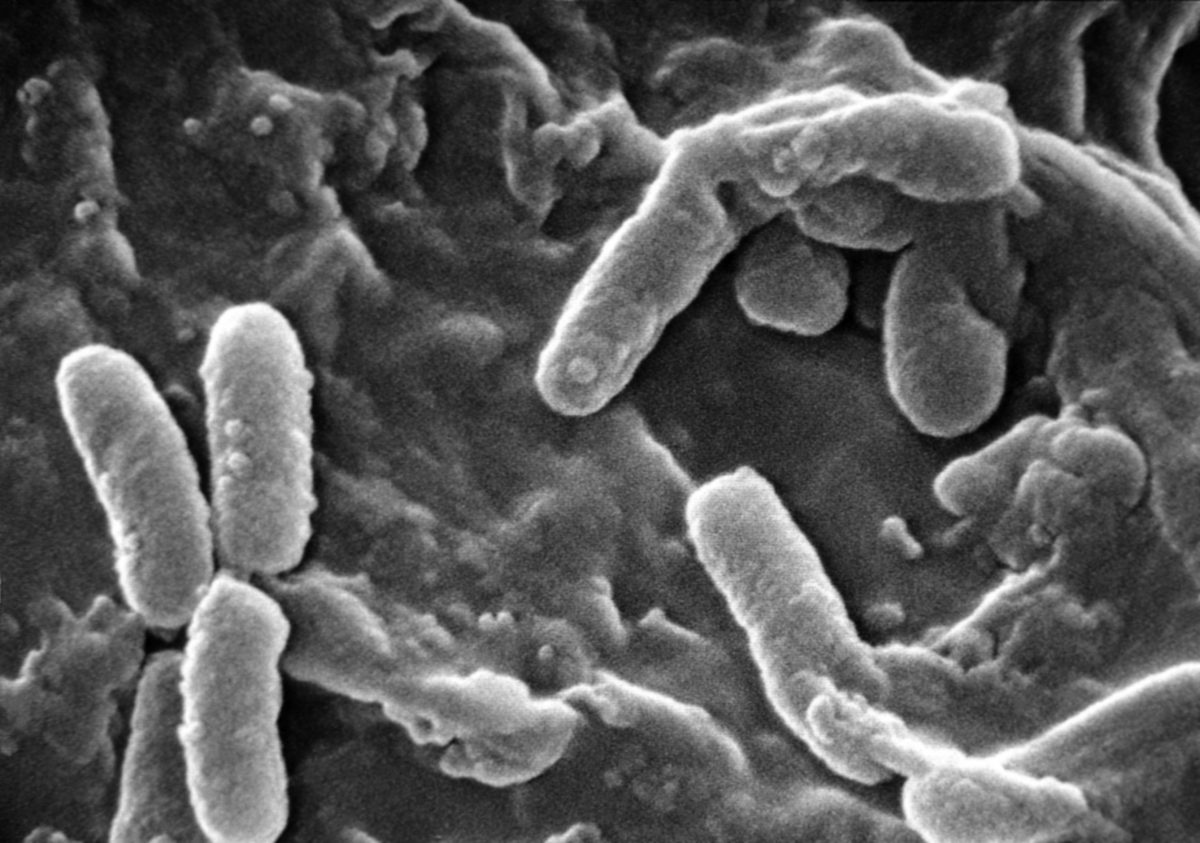
A carbapenem-rezisztens P. aeruginosa egyre növekvő probléma a kórházi körülmények között, amelyek kiváló lehetőségeket kínálnak a gyógyszer-ellenállás terjedésére.
Technológiai korlátok
Noha a korábbi tanulmányok lehetővé tették számunkra, hogy a P. aeruginosa karbapenem-rezisztenciáért felelős génjeit klinikai izolátumokban tanulmányozzuk, a szekvenálási technológia korlátozottságai miatt kevésbé értjük a gének terjedését, különös tekintettel a plazmidok szerepére.
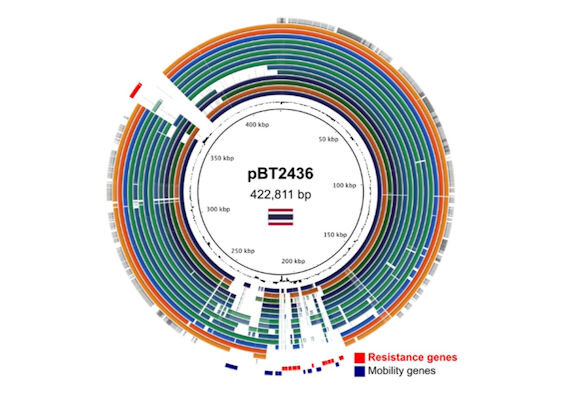
A long-read sequencing felhasználásával a kutatók elolvasták két szoros rokonságban álló megaplazmid teljes génszekvenciáját (> 420 kb), amelyek nagy mennyiségű antibiotikum-rezisztencia gént tartalmaztak, kiterjedt sokszorosítási és rekombinációs események bizonyítékaival.
Az adatbázisokban tárolt DNS-szekvenciák elemzése rámutatott arra, hogy a szóban forgó megaplazmid család a klinikai, környezeti és földrajzi forrásokban, és több faj gazdaszervezetében is jelen van.
A rendelkezésre álló adatbázisok elemzéséből megállapíthatóan, a megaplasmid család története arra utal, hogy a több rezisztenciagént hordozó tagok legalább az 1970-es évek óta megjelentek.
Craig Winstanley professzor, aki a Liverpool Egyetemen végzett kutatást vezette elmondta:
"Az antimikrobiális rezisztencia hatalmas jelentőségű globális kérdés. Ha be akarunk avatkozni a folyamatba, annak ellenőrzésére, akkor alapvető fontosságú, hogy megértsük, hogyan fejlődik és terjed ez az ellenállás. A vizsgálataink azt demonstrálják, hogy a legjobb nagy felbontású szekvenálási és adatelemzési eljárások alkalmazása, a meglévő adatbázisok hatalmas adatmennyiségén, rendkívül fontos a korábban rejtett titkok feltárására."
Dr. Adrian Cazares, aki az adatelemzés nagy részét, és a kutatás társvezetését végezte kijelentette:
"A baktériumok hihetetlenül alkalmazkodó organizmusok, amelyek bármely rendelkezésre álló eszközt felhasználnak. A kutatás megmutatta, hogy a plazmidok formájában - amelyek lehetővé teszik számukra több rezisztenciagén összegyűjtését és az életveszélyes fertőzéseket okozását klinikai körülmények között - hatékony eszközöket találtak."
"Ennélfogva a környezet és a klinikum közötti kapcsolatok felfedezése és megcélzása kulcsfontosságú a jobb antimikrobiális beavatkozások megtervezésében” - mondta a kutató.
(Forrás: Phys.org Képek: Wikipedia, Pixnio)
Itt állíthatod be, hogy a Rakéta az elsők között legyen a Google keresőben